Neue long-read Sequenziertechnologie ermöglicht die Identifikation neuer Krankheitsursachen bei seltenen Erkrankungen
Alle Prozesse in unserem Körper und jeder einzelnen Zellen, werden direkt oder indirekt durch unser Erbgut, die DNA (Desoxyribonukleinsäure), gesteuert. Kommt es zu Veränderungen in der DNA, kann dies verschiedenste Erkrankungen, z.B. Entwicklungsverzögerungen, Neuropathien oder Tumorprädispositionen, zur Folge haben. Neue Verfahren zur DNA-Analyse, die sogenannte long-read Sequenzierung(LRS), erlaubt uns, diese Veränderungen besser zu verstehen und neue Krankheitsursachen zu finden.
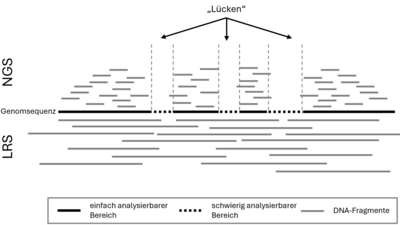
Abbildung 1: Vergleich NGS und LRS. Durch die wesentlichen längeren DNA-Fragmente, die beim LRS sequenziert werden können, ist es möglich auch schwierig analysierbare Bereiche zu untersuchen. Im Vergleich zum NGS kann das gesamte Genom eines Menschen auf Veränderungen analysiert werden.
Eine umfassende Analyse unserer DNA kann Aufschluss über mögliche Erkrankungen geben, aber auch zum besseren Verständnis von Erkrankungsmechanismen beitragen. Seit den 2000er Jahren ist es möglich, mit dem sogenannten next-generation sequencing (NGS), Millionen bzw. Milliarden von DNA-Abschnitten parallel zu analysieren und somit das ganze Genom eines Menschen zu sequenzieren. Teilweise ist es aber insbesondere bei kurzen Leselängen unmöglich diese DNA-Abschnitte einer Position im Genom zuzuordnen.
Neue LRS-Methoden erlauben nun die vollständige Analyse unseres Genoms und helfen somit dabei, bisher unbekannte Krankheitsursachen und -mechanismen zu entdecken. Im Gegensatz zum NGS sind die DNA-Fragmente, welche analysiert werden, 10.000 bis über 100.000 Basen lang, womit das Zusammenfügen zu einem kompletten Genom wesentlich leichter ist.
LRS bietet somit die Möglichkeit mehr Veränderungen in unserem Genom zu erkennen und Krankheitsursachen besser identifizieren und Krankheitsmechanismen besser verstehen zu können. Zusätzliche können kleine Markierungen an den DNA-Basen, die DNA-Methylierungen, mittels LRS gelesen werden. Diese enthalten Informationen über die Aktivität von Genen und können bei bestimmten Erkrankungen (z.B. Imprinting Erkrankungen) verändert sein. Eine LRS Methode ist die Nanopore-Sequenzierung, bei der die DNA durch eine winzige Pore gefädelt und dabei die DNA-Sequenz analysiert wird.
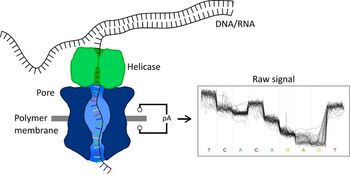
Abbildung 2: Prinzip der Nanopore-Sequenzierung. Die DNA wird mithilfe der Helicase durch eine Proteinpore, geführt und es wird dabei eine Spannung über die Membran angelegt. Der resultierende Ionenfluss wird durch die in der Pore befindlichen Basen gestört. Diese Änderung im Ionenstrom kann gemessen werden und ist charakteristisch für die einzelnen Basen, die sich gerade in der Pore befinden.
Kooperationspartnern nutzen wir die Technologie aber auch für Einzelzelltrankriptomanalysen, de novo Assemblierungen von mikrobiellen Genomen, Splicing Analysen und zur Untersuchung von Methylierungsveränderungen in Tumoren oder bei der Kalzifikation von Blutgefäßen (RWTH OPSF677).
Im Zuge des lonGER Projektes arbeiten wir mit drei Unikliniken in Deutschland und Oxford Nanopore Technologies an einer Implementierung der Nanopore-Sequenzierung in der Krankenversorgung. Als ein Standort des West German Genom Center bieten wir unsere Expertise im Bereich Nanopore-Sequenzierung für Forscher und Forscherinnen deutschlandweit an.
Ansprechpersonen

Dr. rer. nat. Florian Kraft
fkraftukaachende

Univ.-Prof. Dr. med. Ingo Kurth
ikurthukaachende
Publikationen zum Thema
- Genetic landscape of congenital insensitivity to pain and hereditary sensory and autonomic neuropathies
- Closing the Gap - Detection of 5q-Spinal Muscular Atrophy by Short-Read Next-Generation Sequencing and Unexpected Results in a Diagnostic Patient Cohort
- Unstable TTTTA/TTTCA expansions in MARCH6 are associated with Familial Adult Myoclonic Epilepsy type 3